Vil gjenreise effekten av antibiotika

– Vi har tatt opp kampen mot et av verdens største problem, nemlig farlige bakteriers stadig økende evne til å motstå antibiotika, sier kjemiker ved UiT Susann Skagseth. Hun har funnet en forbindelse som kan blokkere resistens hos blant annet sykehusbakterien Klebsiella pneumoniae.
Skagseth har i et doktorgradsprosjekt jobbet tett sammen med mikrobiologer ved Universitetssykehuset i Nord-Norge (UNN). Deres felles målsetning har vært å komme til bunns i noe av problematikken rundt antibiotikaresistens. UNN besitter en unik samling av superresistente bugs fra hele landet, noe som gir gode muligheter til å teste effekt av nye medisiner på noen av de resistente «verstingene».
Det er ikke nok å redusere bruken av antibiotika (Aftenposten 28.03.17)
Skagseth forklarer at bakterier har funnet flere måter å forsvare seg mot antibiotika på. Feilaktig og for mye bruk av særlig penicillin-liknende stoffer har gjort at bakterier som blir resistente mot denne type antibiotika har fått et konkurransefortrinn.
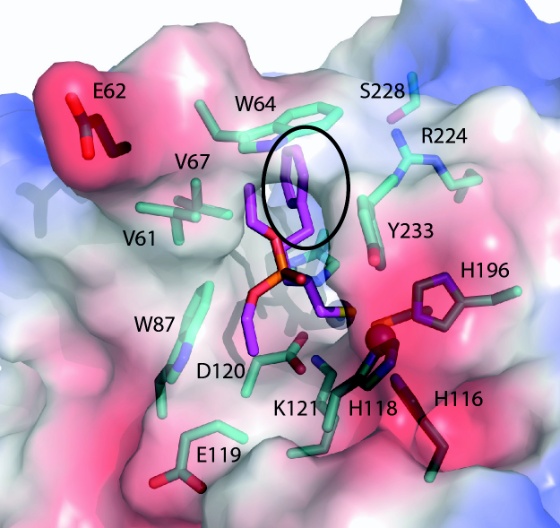
Sykehusbakteriers våte drøm
Konkurransefortrinnet heter beta-lactamaser og er sykehusbakteriers våte drøm, med dette våpenet kan for eksempel Klebsiella pneumoniae etablere seg i lungene i trygg forvissning om at tradisjonelle antibiotika ikke biter.
Antibiotikamisbruk
Noe av det som har utløst denne oppblomstringen av resistens, er utstrakt bruk av antibiotika i dyrefor. Uskyldige bakterier som tåler antibiotika øker i antall og konkurrerer ut de som ikke tåler det.
I tillegg er det slik at genene som koder for beta-lactamaser relativt enkelt kan hoppe over fra en bakterie til neste, og med det spre resistens fra uskyldige bakterier på høns og gris til sykdomsfremkallende utysker.
Ifølge kjemikeren kan antibiotika deles inn i 15 klasser etter måten de dreper bakterier på, og innen hver klasse finnes det mellom en og fire ulike stoffer som er tilgjengelig for medisinsk bruk i dag, men verktøykassen minker. Skagseth har studert Carbapenemer, som er en av medisinene som befinner seg i samme klasse som det mer kjente penicillinet. Det er også mot denne type antibiotika at bakterier har klart å utvikle mest motstandskraft. Penicillin-liknende stoffer har vært lenge i bruk – og lenge misbrukt.
Ødelegger celleveggen
Felles for denne klassen antibiotika er at de angriper det/proteinene/enzymene som skal bygge opp bakteriens cellevegg, noe som igjen fører til at bakterien går i oppløsning. Slik er det også med Skagseth sitt forskningsobjekt, Carbapenem klistrer seg fast til komponenter i celleveggen til bakterier og gjør at nye cellevegger ikke kan ferdigstilles. Men, mange bakterier er nå i stand til å nøytralisere Carbapenem ved hjelp av en type enzymer som kan tygge opp antibiotika, nemlig de nevnte beta-lactamase enzymene.
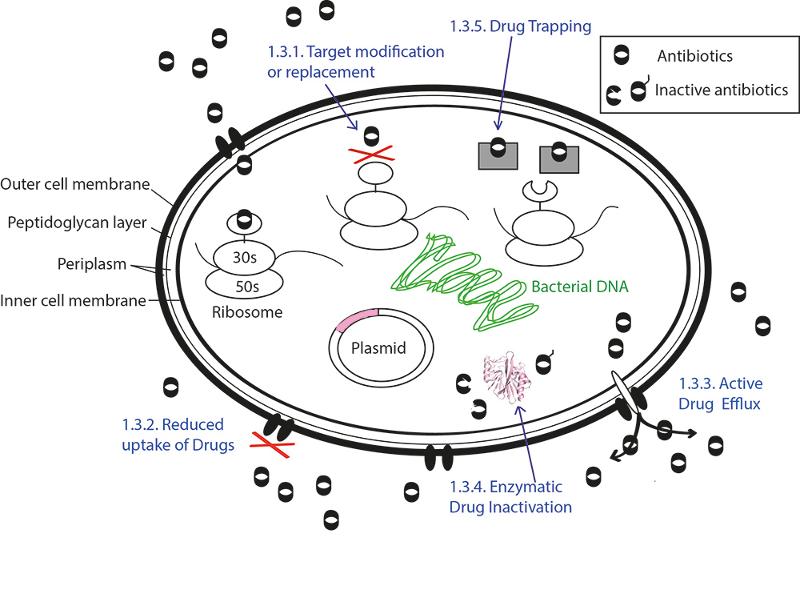
På sporet av et våpen som kan blokkere resistens
Det er her Skagseth har rettet skytset sitt, hun vil eliminere beta-lactamaser slik at antibiotika kan få gjøre jobben sin i fred. I sitt arbeid har hun testet ut ulike inhibitorer som kan blokkere og hemme enzymet sin destruktive effekt.
– Vi har gått løs på resistensproblematikken fra to vinkler; vi har kartlagt hvilke aminosyrer i beta-lactamasene som er viktigst for resistens og vi har testet inhibitorer som er skreddersydd for å blokkere funksjonen til beta-lactamasene.
– Dersom vi skal bevege oss helt ned på det detaljnivået jeg har befunnet meg de siste årene, så må vi forflytte oss innover fra enzymets overflate og inn til molekylets sentrale maskineri. Vi har testet nøyaktig hvilke deler av beta-lactamaser, som er viktig for dets funksjon. Dette detaljnivået har vi oppnådd ved bruk av røntgenkrystallografi, en teknikk for «mikroskopering» på atomnivå og bioteknologiske teknikker for editering av DNA-koden.
Viktig funn
– Vi fant ut at noen aminosyrer hadde en klart viktigere rolle enn andre, hvilket gav oss gode hint om hvilke deler av enzymet vi skulle forsøke å blokkere.
Utgangspunktet for vår design av inhibitorer er en medisin mot høyt blodtrykk, Captopril, som helt overraskende har vist seg å ha effekt også mot resistente antibiotika. Skagseth forteller at gleden var stor da en av inhibitorene som kjemikerne lagde hadde bedre effekt enn andre som var testet tidligere.
– Vi fant en inhibitor som klarer å hindre beta-lactamase enzymene i sitt destruktive arbeid, men det finnes et stort MEN her, felles for våre og andres inhibitorer som blokkerer dette enzymet er at de kan ha negative bivirkninger i kroppen.
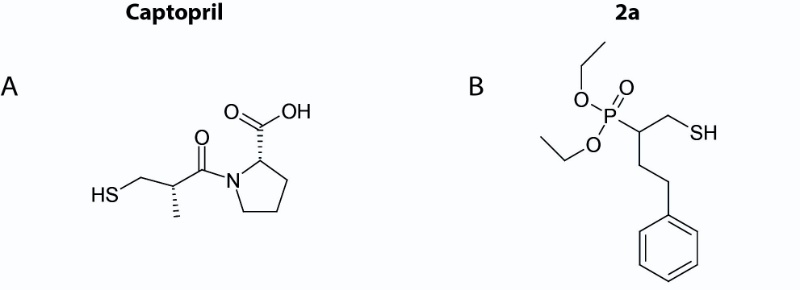
Blokkerer sentrale kroppsfunksjoner i samme slengen
En sentral komponent i inhibitorene er en svovelholdig gruppe, en gruppe som er kjent for å kunne ha negativ effekt ikke bare mot resistente bugs, men også på andre funksjoner i den kroppen som skal medisineres. Svovelgruppen har det til felles at de liker å hekte seg på metallioner som finnes i kroppen og stjeler viktige bestanddeler fra kroppens maskineri.
Uten svovel redusert effekt
Skagseth har også laget inhibitorer uten denne svovelgruppen i håp om å finne et medikament uten alle de negative effektene, men da falt også deres inhiberende effekt.
Nå fortsetter jobben med å videreforedle inhibitorene som blokkerer beta-lactamaser og finne en kandidat som i kombinasjon med penicillin kan bekjempe resistente superbugs i fremtiden, avslutter en kamplysten Skagseth.
Susann Skagseth disputerte 16. Februar med oppgaven: “Mutational, structural and inhibitory investigation of metallo-β-lactamases involved in antibiotic resistance”. Som stipendiat var hun tilknyttet forskerskolen BioStruct - The National graduate school in structural biology og ble veiledet av Hanna Kirsti S. Leiros, Institutt for kjemi, UiT Norges arktiske universitet, Ørjan Samuelsen, UNN og Gro Bjerga, UiT og Uni Research AS.
Les også: Antibiotikaresistens – et økende globalt helseproblem




